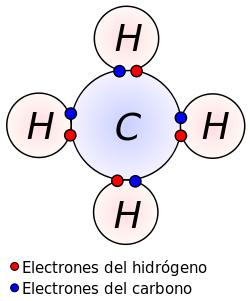
Transformaciones físicas y transformaciones químicas
Fenómenos o Cambios Físicos: Son procesos en los que no cambia la naturaleza de las sustancias ni se forman otras nuevas.
Ejemplos:
Cambios de estado: Si aplicamos una fuente de calor de forma constante, el agua hierve y se transforma en vapor de agua. (En ambos casos, la sustancia implicada en el proceso es agua que, en un caso está líquida y en el otro está gaseosa; esto es, sus partículas están ordenadas de diferente manera según la teoría cinética de la materia).
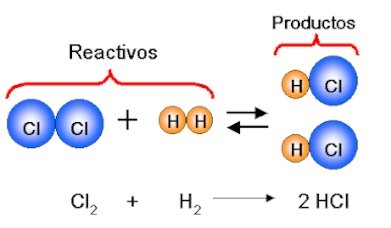
Fenómenos o Cambios Químicos: Son procesos en los que cambia la naturaleza de las sustancias, además de formarse otras nuevas.
Ejemplos:
Combustión: Si quemamos un papel, se transforma en cenizas y, durante el proceso, se desprende humo. (Inicialmente, tendríamos papel y oxígeno, al concluir el cambio químico tenemos cenizas y dióxido de carbono, sustancias diferentes a las iniciales).
Corrosión: Si dejamos un trozo de hierro a la intemperie, se oxida y pierde sus propiedades iniciales. (Las sustancias iniciales serían hierro y oxígeno, la sustancia final es óxido de hierro, con unas propiedades totalmente diferentes a las de las sustancias iniciales).
Número de Avogadro
| Valores de NA[1] | Unidades |
|---|
| 6.022 141 79(30)×1023 | mol−1 |
| 2.731 597 57(14)×1026 | lb-mol.−1 |
| 1.707 248 479(85)×1025 | oz-mol.−1 |
| Para más detalles, ver Terminología y unidades más adelante. |
En
química y en
física, la
constante de Avogadro (símbolos:
L,
NA) es el número de
entidades elementales (normalmente
átomos o
moléculas) que hay en un
mol, esto es (a partir de la definición de mol), el número de átomos de carbono contenidos en 12
gramos de
carbono-12.
[2] [3] Originalmente se llamó
número de Avogadro.
En 2006, la
CODATA recomendó este valor de:
[1]

La constante de Avogadro debe su nombre al científico italiano de principios del siglo XIX
Amedeo Avogadro, quien, en 1811, propuso por primera vez que el volumen de un gas (a una determinada presión y temperatura) es proporcional al número de
átomos, o
moléculas, independientemente de la naturaleza del gas.
[4] El físico francés
Jean Perrin propuso en 1909 nombrar la constante en honor de Avogadro.
[5] Perrin ganaría en 1926
Premio Nobel de Física, en gran parte por su trabajo en la determinación de la constante de Avogadro mediante varios métodos diferentes.
[6]
El valor de la constante de Avogadro fue indicado en primer lugar por
Johann Josef Loschmidt que, en 1865, estimó el diámetro medio de las moléculas en el aire por un método equivalente a calcular el número de partículas en un volumen determinado de gas.
[7] Este último valor, la
densidad numérica de partículas en un
gas ideal, que ahora se llama en su honor
constante de Loschmidt, es aproximadamente
proporcional a la constante de Avogadro. La conexión con Loschmidt es la raíz del símbolo
L que a veces se utiliza para la constante de Avogadro, y la literatura en
lengua germana puede referirse a ambas constantes con el mismo nombre, distinguiéndolas solamente por las
unidades de medida.
[8]
http://es.wikipedia.org/wiki/N%C3%BAmero_de_Avogadro

Un catalizador propiamente dicho es una sustancia que está presente en una reacción química en contacto físico con los reactivos, y acelera, induce o propicia dicha reacción sin actuar en la misma.
Tipos de catálisis
Los catalizadores pueden ser homogéneos o heterogéneos, dependiendo de si existe un catalizador en la misma
fase que el
sustrato. Los
biocatalizadores son vistos a menudo como un grupo separado.
Catalizadores heterogéneo

Catalizadores sólidos heterogéneos como los
convertidores catalíticos de los automóviles están colocados en estructuras diseñadas para maximizar su área superficial.
Los catalizadores heterogéneos son aquellos que actúan en una
fase diferente que los
reactivos. La mayoría de los catalizadores heterogéneos son
sólidos que actúan sobre sustratos en una mezcla de reacción
líquida o gaseosa. Se conocen diversos mecanismos para las
reacciones en superficies, dependiendo de cómo se lleva a cabo la adsorción (
Langmuir-Hinshelwood,
Eley -Rideal, y Mars-van Krevelen).
[8] El área superficial total del sólido tiene un efecto importante en la velocidad de reacción. Cuanto menor sea el tamaño de partícula del catalizador, mayor es el área superficial para una masa dada de partículas.
Catalizadores homogéneos
Normalmente los catalizadores homogéneos están disueltos en un disolvente con los sustratos. Un ejemplo de catálisis homogénea implica la influencia de
H+ en la
esterificación de los ésteres, por ejemplo, acetato de metilo a partir del ácido acético y el metanol.
[9] Para los químicos inorgánicos, la catálisis homogénea es a menudo sinónimo de
catalizadores organometálicos.
[10]
http://es.wikipedia.org/wiki/Cat%C3%A1lisis#Tipos_de_cat.C3.A1lisis
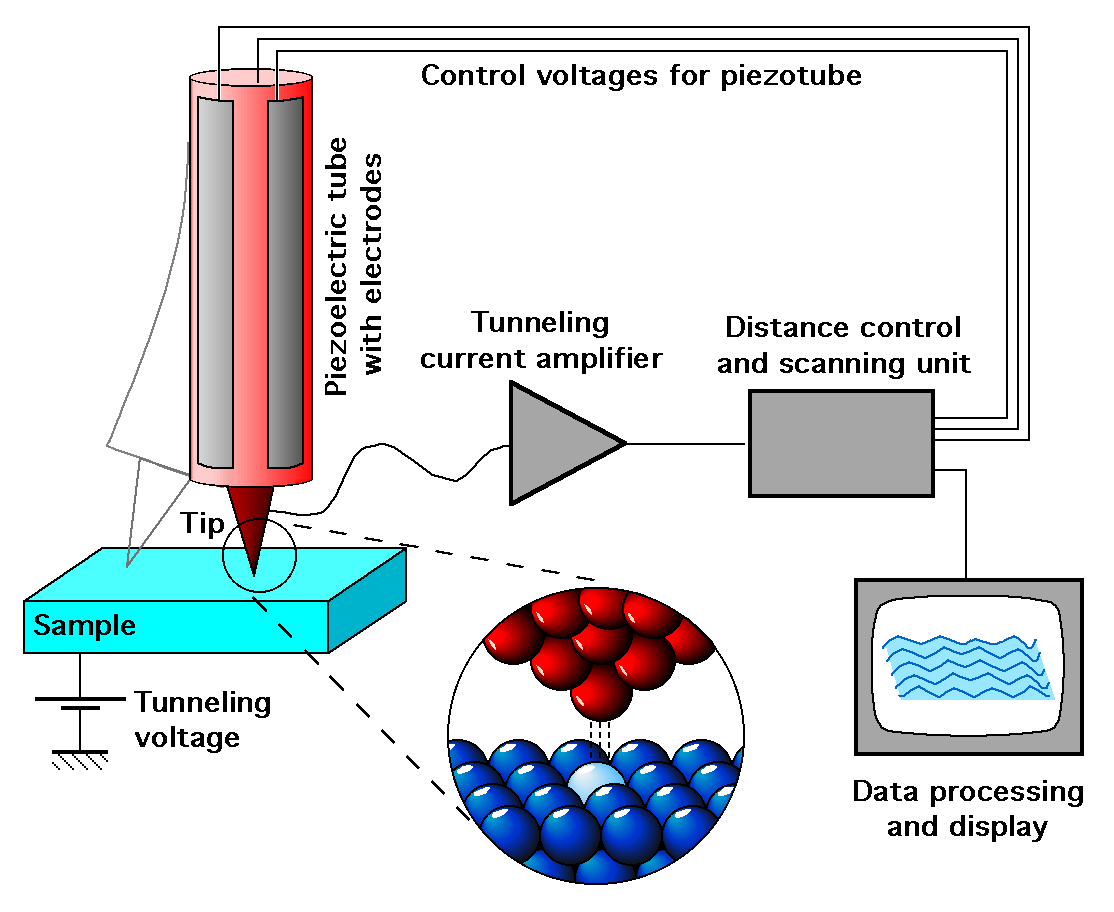
Microscopio de efecto túnel
El
microscopio de efecto túnel (
Scanning Tunneling Microscope STM) o
microscopio ciego es un poderoso instrumento que per
El efecto túnel
Desde el punto de vista de la mecánica clásica un electrón no puede superar una
barrera de potencial superior a su energía.
Sin embargo, según la mecánica cuántica, los electrones no están definidos por una posición precisa, sino por una nube de probabilidad. Esto provoca que en ciertos sistemas esta nube de probabilidad se extienda hasta el otro lado de una barrera de potencial. Por tanto el electrón puede atravesar la barrera, y contribuir a generar una intensidad eléctrica.
Esta intensidad se denomina intensidad de túnel y es el parámetro de control que nos permite realizar la topografía de superficie.
Este efecto cuántico aparece también en otras ramas de la física.
Gamow lo aplicó para dar explicación a la desintegración mediante emisión de partículas alfa en núcleos inestables. En electrónica, hay
transistores que basan parte de su funcionamiento en el efecto túnel.
mite visualizar superficies a escala del
átomo.
 http://es.wikipedia.org/wiki/Microscopio_de_efecto_t%C3%BAnel
http://es.wikipedia.org/wiki/Microscopio_de_efecto_t%C3%BAnel
El
mol (símbolo:
mol) es la
unidad con que se mide la
cantidad de sustancia, una de las siete
magnitudes físicas fundamentales del
Sistema Internacional de Unidades.
Dada cualquier sustancia (elemento químico, compuesto o material) y considerando a la vez un cierto tipo de entidades elementales que la componen, se define como un mol a la cantidad de esa sustancia que contiene tantas entidades elementales del tipo considerado, como
átomos hay en 12
gramos de
carbono-12. Esta definición no aclara a qué se refiere con
cantidad de sustancia y su interpretación es motivo de debates,
[1] aunque normalmente se da por hecho que se refiere al número de entidades.
El número de unidades elementales –
átomos,
moléculas,
iones,
electrones,
radicales u otras partículas o grupos específicos de éstas– existentes en un
mol de sustancia es, por definición, una constante que no depende del material ni del tipo de partícula considerado. Esta cantidad es llamada
número de Avogadro (N
A)
[2] y equivale a:
Microscopio
El microscopio (de micro-, μικρο, pequeño, y scopio, σκοπεω, observar) es un instrumento que permite observar objetos que son demasiado pequeños para ser vistos a simple vista. El tipo más común y el primero que se inventó es el microscopio óptico. Se trata de un instrumento óptico que contiene una o varias lentes que permiten obtener una imagen aumentada del objeto y que funciona por refracción.
La ciencia que investiga los objetos pequeños utilizando este instrumento se llama microscopía.